Cómo el ejercicio físico transforma tu cuerpo: el músculo esquelético y su relación con la quinurenina

Autor Chimalli Digital
El músculo esquelético, uno de los órganos más grandes y el motor del aparato locomotor de nuestro cuerpo, representa hasta el 40% de la masa corporal en un individuo delgado.
En conjunto con el hígado, nuestros músculos absorben la mayor parte de la glucosa postprandial en respuesta a los estímulos de la insulina y contribuyen significativamente a mantener la temperatura corporal.
Adicionalmente, los músculos esqueléticos constituyen una gran reserva de aminoácidos que, en condiciones críticas, pueden ser desplazados para la producción de energía por diversos órganos.
El músculo esquelético es un órgano con mucha plasticidad, cuya composición y rendimiento pueden cambiarse a través del ejercicio físico.
Y es que los beneficios del ejercicio van más allá de los límites de la función muscular y la homeostasis energética sistémica e incluyen, entre ellos, mejoras en la plasticidad cerebral y la cognición.
Por dicha razón, el ejercicio físico puede utilizarse para prevenir y/o tratar enfermedades como la diabetes tipo 2, el cáncer de mama y de colon, la depresión, el cáncer caquexia y sarcopenia.
Ejercicio Físico VS Actividad Física: ¿Cuál es la diferencia y cuál es mejor para tu salud?

Si bien aún la comunidad científica no comprende del todo los mecanismos por los cuales el ejercicio físico produce varios de sus beneficios en el cuerpo humano, resulta importante enfatizar que, aunque tanto la actividad física como el ejercicio físico son beneficiosos para la salud, no son lo mismo y pueden implicar vías moleculares muy diferentes.
La actividad física se define como cualquier movimiento en el que intervienen músculos esqueléticos y que da lugar a un gasto energético, incluidas las actividades de la vida diaria.
En cambio, el ejercicio físico se refiere a movimientos planificados, estructurados y con frecuencia repetitivos cuyo objetivo es mejorar o mantener un determinado nivel de rendimiento.
El ejercicio físico tiene beneficios específicos para la salud humana y puede utilizarse para mejorar diferentes afecciones.
El entrenamiento de resistencia aumenta la eficiencia energética muscular, la capacidad oxidativa, la resistencia a la fatiga y la función cardiovascular, mientras que el entrenamiento de fuerza produce hipertrofia muscular y puede utilizarse para tratar la sarcopenia.
A la postre, comúnmente se usa el término “agudo” para describir una única sesión de ejercicio y “crónico” para describir una rutina de ejercicio prolongada.
Al margen de su importancia para la locomoción y el uso de la energía, el músculo esquelético es cada vez más apreciado como órgano endocrino con capacidad para secretar diversas citoquinas (mioquinas).
Dichos metabolitos y proteínas desempeñan efectos autocrinos, paracrinos o endocrinos y afectan al metabolismo, la inflamación y la proliferación celular, entre otros procesos.
El poder de la adaptación muscular

Para hacer frente a los desafíos del ejercicio físico repetido, las fibras musculares experimentan adaptaciones estructurales y metabólicas para asegurarse de que se suministra el combustible adecuado en la cantidad correcta para alimentar el aparato contráctil.
El musculo esquelético está compuesto por diferentes tipos de fibras, cuya nomenclatura se clasifica en función de su estructura metabólica y del tipo de cadena pesada de miosina expresada.
Los dos extremos de los tipos de fibras se encuentran representados por las fibras glucolíticas, de alto desarrollo de fuerza, de contracción rápida y fatigables de tipo IIB, frente a las fibras oxidativas, resistentes a la fatiga, de contracción lenta y de bajo desarrollo de fuerza de tipo I.
Dichas fibras están optimizadas para utilizar diferentes tipos de combustible.
Las fibras de tipo IIB tienen mayores niveles de almacenamiento de glucógeno y pueden generar más ATP a partir de la glucólisis (en comparación con las de tipo I) debido a una mayor actividad de la deshidrogenasa láctica, una mayor actividad de la lanzadera de glicerol-3-fosfato y mayores niveles de fosfofructocinasa/fructosa-bifosfatasa 3.

Por otra parte, las fibras de tipo I tienen mayores reservas de lípidos y una expresión elevada de lipasas para utilizar los ácidos grasos para la fosforilación oxidativa.
Es posible hacer uso de diversos programas de entrenamiento para mejorar aspectos concretos de la función muscular.
Dichas adaptaciones duraderas inducidas por el entrenamiento implican cambios en la expresión de redes de genes coordinadas por factores de transcripción y correguladores.
Los factores de transcripción responden a estímulos específicos y pueden regular directamente la expresión de genes implicados en la adaptación a dicho estimulo.
No obstante, para que la fibra muscular se adapte funcionalmente a un nuevo nivel de rendimiento, se requiere un alto nivel de coordinación entre la inervación, la vascularización, el metabolismo energético, el manejo del calcio y la expresión del aparato contráctil adecuado.
Por dicha razón, la regulación de la expresión génica mediada por coactivadores ha surgido como un mecanismo importante en la adaptación muscular al ejercicio, al garantizar que la actividad de los diferentes factores de transcripción se potencie de forma coordinada.
Ejercicio Físico y cambios en la masa muscular: el papel de los coactivadores del receptor-γ activado por el proliferador de peroxisomas

La familia de coactivadores transcripcionales (PGC) del receptor-γ activado por el proliferador de peroxisomas es importante para la función del músculo esquelético y la adaptación al ejercicio físico crónico.
La familia incluye PGC-1α, PGC-1 β y PGC-coactivadores relacionados (PRC), que potencian la actividad de los receptores de hormonas nucleares y otros factores de transcripción.
PGC-1α es el miembro más estudiado por la comunidad científica y está altamente regulado en un contexto y tejido especifico.
Por ejemplo, la expresión de PGC-1α en el músculo esquelético es inducida por el ejercicio físico agudo y crónico, mientras que en el hígado responde al ayuno.
Curiosamente, el gen PGC-1α se expresa como una colección de variantes de empalme que codifican proteínas con diferentes actividades biológicas.
PGC-1α1 representa la variante canónica de transcripción más larga, identificada inicialmente como un gen inducible por el frio que se expresa en el tejido adiposo marrón.
PGC-1α2 y PGC-1α3 están implicados en la regulación del acoplamiento alternativo, y PGC-1α4 es el transcrito más corto conocido de la familia, activado principalmente durante el ejercicio de fuerza, proporcionando adaptaciones que conducen al aumento de la masa muscular y la fuerza.
El fenotipo hipertrófico se consigue principalmente mediante la inducción de IGF-1 y la represión de la expresión de miostatina.

En el músculo esquelético, la activación de PGC-1α1 impulsa un programa genético que fomenta el cambio de tipo de fibra, la angiogénesis y la biogénesis mitocondrial, proporcionando la adaptación estructural y funcional al ejercicio de resistencia.
La actividad de PGC-1α1 también está implicada en la regulación de numerosas vías metabólicas, como el metabolismo de los aminoácidos de cadena ramificada, el metabolismo de la alanina, la vía de las pentosas fosfato, la oxidación de ácidos grasos, el ciclo del TCA y otras.
Resulta importante enfatizar que, aparte de regular las adaptaciones locales en las fibras musculares donde se inducen, los coactivadores PGC-1α también controlan la expresión y liberación de diversas mioquinas como la irisina, el ácido β-aminoisobutírico (BAIBA), meteroin-like, neurturina y la IL-6.
La liberación de estos receptores es mayor tras el ejercicio agudo y la comunidad científica cree que desempeñan un rol importante en la interacción entre el músculo y otros órganos.
Aumento de masa muscular: explorando el papel de la vía de la quinurenina en el metabolismo del triptófano

El triptófano (Trp) es un aminoácido esencial necesario para la síntesis de proteínas y tiene dos vías de degradación esenciales.
La primera de ellas es hacía la biosíntesis de la serotonina y su derivado la melatonina, que intervienen en la regulación del estado de ánimo y el sueño, respectivamente.
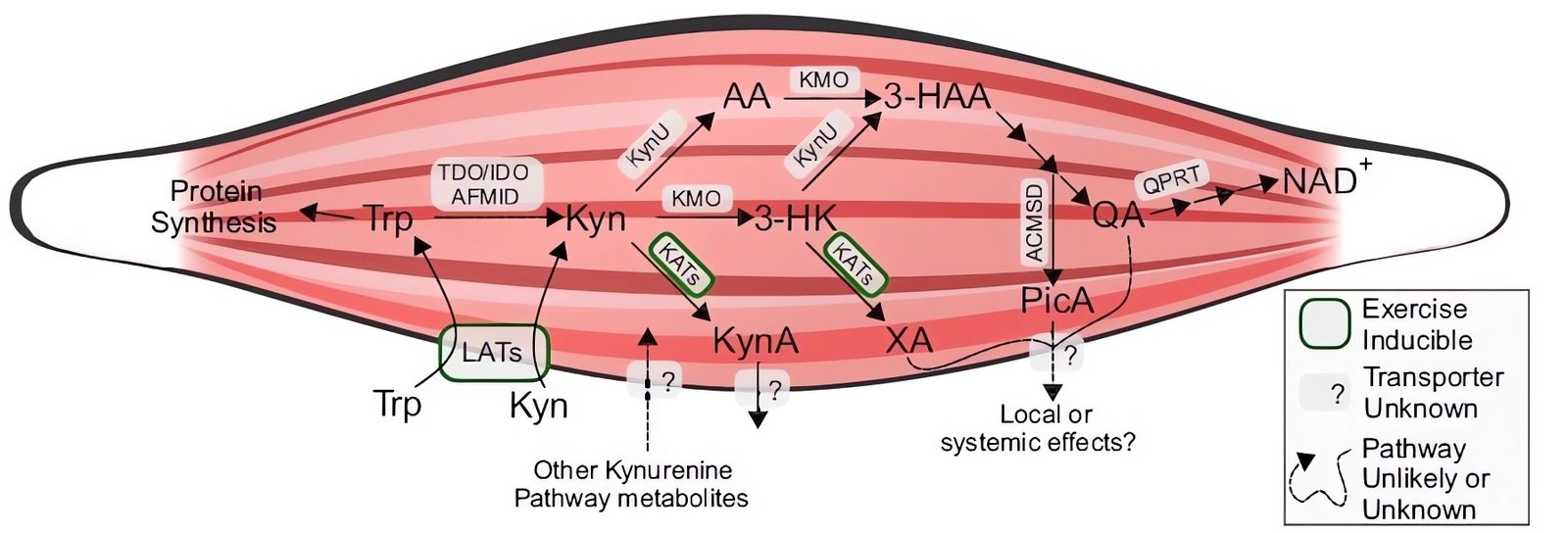
La segunda es la vía de la quinurenina, que puede conducir a la formación de nicotinamida adenina dinucleótido (NAD+).
La vía de la quinurenina incluye diversas enzimas que degradan el 95% del triptófano libre en varios metabolitos bioactivos de la vía de la quinurenina (KPM), con frecuencia denominadas quinureninas.
La quinurenina (Kyn) es el primero de muchos metabolitos bioactivos de la vía de la quinurenina, que han demostrado estar implicados en la modulación de los sistemas inmunitario y nervioso central.
Por dicha razón, la Kyn y los KPM han sido estudiados especialmente en el contexto del cáncer y las enfermedades psiquiátricas.

La conversión de triptófano en Kyn requiere las enzimas triptófano 2,3-dioxigenasa (TDO) o indoleamina 2,3-dioxigenasa (IDO) y quinurenina formamidasa y ocurre principalmente en el hígado.
No obstante, cuando los niveles de cortisol y citoquinas inflamatorias son elevados, la expresión de la TDO hepática se reprime y se induce la IDO de las células inmunitarias.
Esto desplaza la producción de Kyn al compartimento inmunitario como parte de un bucle de retroalimentación negativa para controlar las respuestas inflamatorias.
En el músculo esquelético hay poca expresión de IDO y una actividad enzimática mínima de TDO, por lo que es más probable que la Kyn se produzca en el hígado (o en las células inmunitarias) y luego se importe a las fibras musculares.
A continuación, la Kyn puede metabolizarse en ácido quinurénico (KynA), ácido antranílico (AA) o 3-hidroxi-L-quinurenina (3-HK).
Curiosamente, el eje PGC-1α1/PPARα/δ en el músculo aumenta la expresión de las quinureninas aminotransferasas (KATs), que convierten la Kyn en KynA.
Dichas enzimas pertenecen a la vía de la quinurenina de la degradación del triptófano y se ha demostrado que aumentan en el músculo esquelético tras el ejercicio tanto en ratones como en humanos.
Algunos de los compuestos de la vía de la quinurenina son metabolitos finales y otros pueden seguir procesándose hasta convertirse en NAD+.
No obstante, con excepción de los hepatocitos, existen pocas células en el organismo que estén totalmente equipadas con la maquinaria enzimática necesaria para llevar a cabo por completo la degradación de Trp a NAD+.
Esto convierte a los KPM en excelentes candidatos a mediadores de la comunicación cruzada entre células u órganos, ya que pueden intercambiarse entre tejidos para continuar su viaje por la vía o ejercer un efecto biológico.
La actividad biológica de muchos de estos metabolitos está bien establecida en el sistema nervioso central, mientras que en la periferia se sabe menos.
La clave para la comunicación entre órganos después del ejercicio físico: metabolitos de la vía de la quinurenina

El vínculo entre el músculo esquelético, el ejercicio y las KPM surgió de la observación de que el músculo ejercitado (o el músculo con altos niveles de PGC-1α1) tiene niveles muy altos de enzimas KAT.
Esto mejora la conversión periférica de Kyn en KynA y evita la acumulación de Kyn en el cerebro, que se observa en ciertos trastornos mentales como la depresión inducida por el estrés.
En ratones, dicho mecanismo reduce la excitotoxicidad relacionada con la Kyn, la neuroinflamación y los comportamientos de tipo depresivo.
Dado que la activación de dicha vía depende en gran medida de PGC-1α1, los ratones modificados genéticamente para carecer de la expresión de este coactivador en el músculo muestran un comportamiento de tipo depresivo y una menor capacidad para catabolizar la Kyn, incluso ante la ausencia de cualquier tipo de desafío.
Situación que puso de manifiesto que el músculo esquelético y el ejercicio físico son reguladores del metabolismo del Trp-Kyn, con importantes consecuencias sistémicas.
Aunque los científicos saben que el KynA plasmática, pero no la Kyn, aumenta tras el ejercicio físico, todavía desconocen cómo sale la KynA de las fibras musculares o si otras KPM se elevan tras el ejercicio (ya sea intramuscularmente o en la circulación).
Ejercicio Físico: efectos del ejercicio en la respuesta inmunológica y la composición y función del tejido adiposo

Dado que la elevación del KynA circulante tras el ejercicio físico está impulsada por el músculo esquelético, estudios científicos posteriores se enfocaron en investigar si el KynA puede funcionar como mioquina.
De hecho, la elevación diaria del KynA a niveles postejercicio en ratones durante un periodo de 1 a 4 semanas produjo pérdida de peso debido a la reducción de la adiposidad.
Curiosamente, la pérdida de peso no se debió a cambios en la ingesta de alimentos, sino a un aumento del gasto energético del tejido adiposo mediado por la inducción de adipocitos beige en los depósitos adiposos subcutáneos y visceral (un fenómeno conocido como pardeamiento del tejido adiposo).
Los adipocitos beige son capaces de “desperdiciar” energía vinculando la oxidación de ácidos grasos a ciclos fútiles que disipan energía en forma de calor.

La administración del KynA a ratones también cambió la firma celular inmunitaria dentro del tejido adiposo, que pasó a un fenotipo más antiinflamatorio.
Los efectos observados del KynA fueron mediados por la señalización del receptor 35 acoplado a proteína G (GPR35), y la subsiguiente regulación al alza de PGC-1α1.
Resulta importante enfatizar que los ratones modificados genéticamente GPR35 son resistentes a el KynA o al pardeamiento por el ejercicio físico inducido del tejido adiposo.
Esto apoya aún más el papel del KynA como mioquina inducida por el ejercicio físico con efectos sobre el gasto energético sistémico y el control del sistema inmunitario.
Aparte del GPR35 existen otros receptores KPM expresados en diferentes tejidos periféricos. Esto sugiere que otras KPM también podrían ser mioquinas.
Comparte en tus redes sociales:
TE AGRADECEMOS QUE HAYAS LLEGADO HASTA AQUÍ, Y TE INVITAMOS A QUE NOS COMPARTAS TU OPINIÓN EN LA CAJA DE COMENTARIOS.
Artículos Recomendados
¿Qué es la aterosclerosis?
Conoce los principales factores de riesgo y cómo prevenirla
🟡 🩸 La aterosclerosis es la acumulación de material graso y/o fibroso en la capa más interna de las arterias, la íntima. 🫀
🚨 🛑 El termino aterosclerosis se deriva de las palabras griegas “athera”, comida triturada en forma de masa, “scleros”, duro, y el sufijo “osis”, conversión/formación. Por lo que etimológicamente se podría entender cómo; formación de comida triturada en forma de masa dura. 🟡 🩸

LA CIENCIA DEL CALENTAMIENTO: CÓMO OPTIMIZAR EL RENDIMIENTO DEPORTIVO CON TÉCNICAS EFECTIVAS

¿CÓMO FUNCIONA LA RESPIRACIÓN DURANTE EL EJERCICIO FÍSICO? DESCUBRE LOS ÚLTIMOS HALLAZGOS CIENTÍFICOS

CALAMBRES MUSCULARES: ¿POR QUÉ OCURREN? ¿SOLO MOLESTOS O SÍNTOMAS DE ALGO MÁS GRAVE?

TODO SOBRE LA CREATINA: ¿QUÉ ES? ¿CÓMO FUNCIONA? ¿PARA QUÉ SIRVE? ¿ES SEGURA?

ENTRENAMIENTO HIIT: LA CLAVE PARA MEJORAR TU SALUD CARDIOVASCULAR RÁPIDAMENTE

¿POR QUÉ SUDAMOS? SUDOR, MECANISMO CRUCIAL PARA PRESERVAR TU BIENESTAR

¿POR QUÉ SIENTES FATIGA AL HACER EJERCICIO? LA CIENCIA DETRÁS DEL CANSANCIO